Leg uit waarom het een breed gebied is en geen scherpe piek. Leg deze getallen uit op basis van het uitsluitingsprincipe van Pauli en het begrip spin. Leid deze formule af met behu... Leg uit waarom het een breed gebied is en geen scherpe piek. Leg deze getallen uit op basis van het uitsluitingsprincipe van Pauli en het begrip spin. Leid deze formule af met behulp van formules uit Binas. Toon met een berekening aan dat het eendimensionale doosjesmodel voor dit molecuul redelijk voldoet.
Understand the Problem
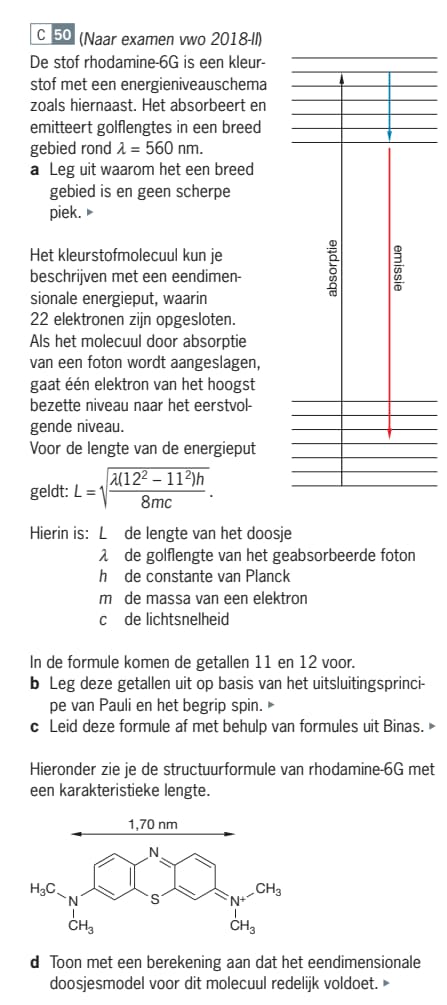
De vraag gaat over de stof rhodamine-6G en vraagt om uitleg over een breed absorptiegebied en een aantal berekeningen met betrekking tot de energie van een elektron in een doosje. De student moet de eigenschappen van het molecuul en de bijbehorende formule verklaren en deze afleiden met behulp van relevante formules uit Binas. Dit is een chemiegerelateerde taak.
Answer
Het brede gebied is door het uitsluitingsprincipe van Pauli en elektronspin, resulterend in diverse energietoestanden.
Het brede gebied komt door de kwantumtoestanden van de 22 elektronen in verschillende energieën. Het uitsluitingsprincipe van Pauli en elektronspin zorgen voor diverse energieniveaus, wat een breed spectrum oplevert. De formule met L beschrijft dit, gebaseerd op de elektronlengte en het eendimensionale doosjesmodel.
Answer for screen readers
Het brede gebied komt door de kwantumtoestanden van de 22 elektronen in verschillende energieën. Het uitsluitingsprincipe van Pauli en elektronspin zorgen voor diverse energieniveaus, wat een breed spectrum oplevert. De formule met L beschrijft dit, gebaseerd op de elektronlengte en het eendimensionale doosjesmodel.
More Information
Het uitsluitingsprincipe van Pauli stelt dat geen twee identieke fermionen, zoals elektronen, dezelfde kwantumtoestand kunnen delen. Dit principe, samen met elektronspin, veroorzaakt een spreiding in energieniveaus, wat leidt tot een breder emissiespectrum.
Tips
Een veelgemaakte fout is te denken dat electronen willekeurig energieniveaus bezetten. Ze volgen echter strikt het uitsluitingsprincipe en hebben ook inbreng van hun spin.
Sources
- Uitsluitingsprincipe van Pauli - Wikipedia - nl.wikipedia.org
AI-generated content may contain errors. Please verify critical information