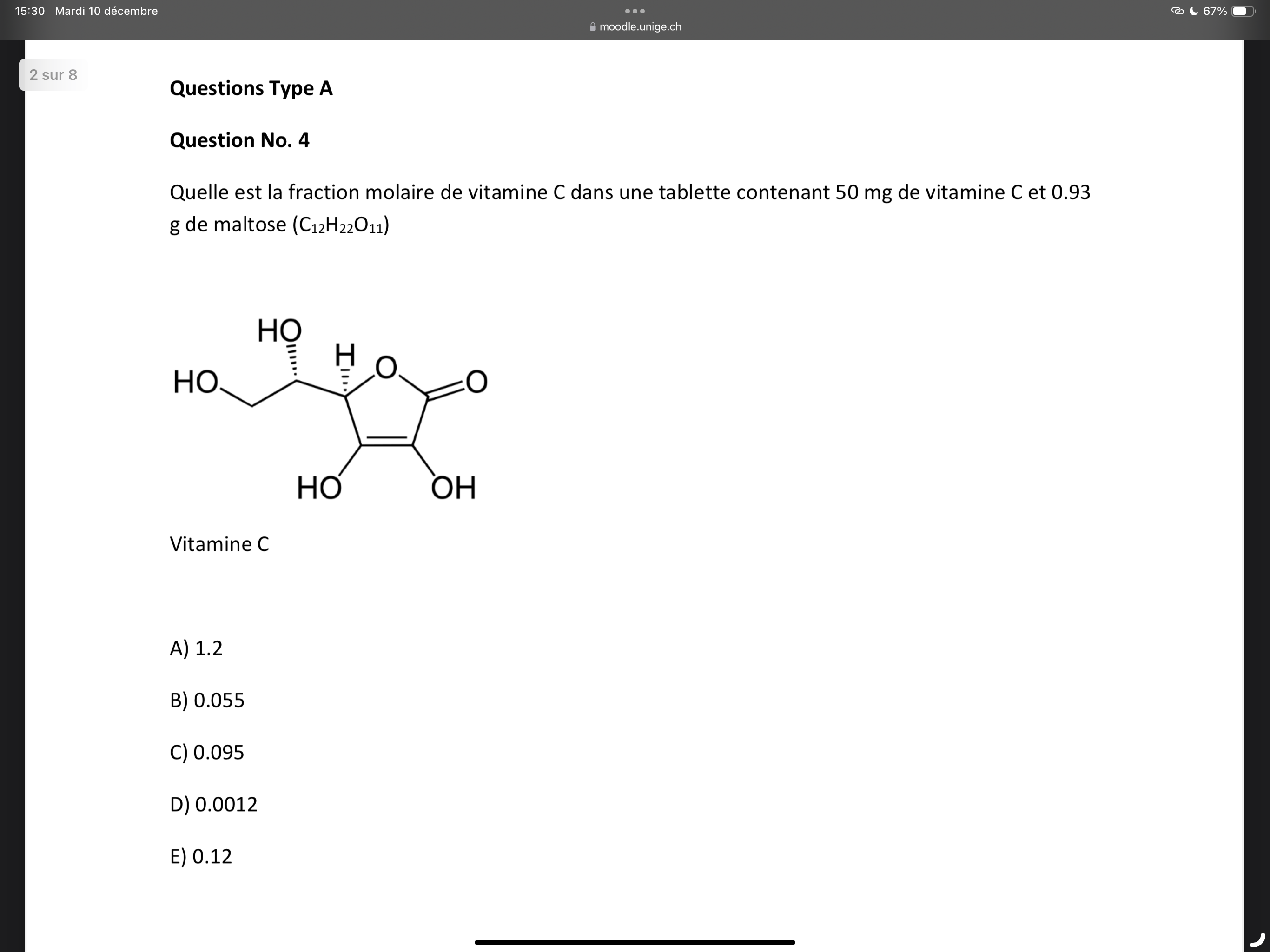
Quelle est la fraction molaire de vitamine C dans une tablette contenant 50 mg de vitamine C et 0.93 g de maltose (C12H22O11) ?
Understand the Problem
La question demande de calculer la fraction molaire de vitamine C dans une tablette, en tenant compte de 50 mg de vitamine C et 0,93 g de maltose. Cela implique l'utilisation de concepts de chimie, tels que les fractions molaires et la conversion des unités.
Answer
La fraction molaire de vitamine C est $0.095$.
Answer for screen readers
La fraction molaire de vitamine C dans la tablette est approximativement $0.095$.
Steps to Solve
- Convert les masses en grammes
Nous avons 50 mg de vitamine C. Pour le convertir en grammes, nous utilisons la conversion suivante :
$$ 50 , \text{mg} = 0.050 , \text{g} $$
- Calculer le nombre de moles de vitamine C
Déterminons la masse molaire de la vitamine C (C₆H₈O₆). La masse molaire est calculée comme suit :
- Carbone (C): 6 atomes × 12.01 g/mol = 72.06 g/mol
- Hydrogène (H): 8 atomes × 1.008 g/mol = 8.064 g/mol
- Oxygène (O): 6 atomes × 16.00 g/mol = 96.00 g/mol
Additionnons ces valeurs :
$$ \text{Masse molaire de C} = 72.06 + 8.064 + 96.00 = 176.124 , \text{g/mol} $$
Maintenant, calculons le nombre de moles de vitamine C :
$$ n_{\text{vitamine C}} = \frac{m}{M} = \frac{0.050 , \text{g}}{176.124 , \text{g/mol}} $$
- Calculer le nombre de moles de maltose
La formule du maltose est C₁₂H₂₂O₁₁. Calculons sa masse molaire :
- Carbone (C): 12 atomes × 12.01 g/mol = 144.12 g/mol
- Hydrogène (H): 22 atomes × 1.008 g/mol = 22.176 g/mol
- Oxygène (O): 11 atomes × 16.00 g/mol = 176.00 g/mol
Additionnons ces valeurs :
$$ \text{Masse molaire de maltose} = 144.12 + 22.176 + 176.00 = 342.296 , \text{g/mol} $$
Maintenant, calculons le nombre de moles de maltose :
$$ n_{\text{maltose}} = \frac{0.93 , \text{g}}{342.296 , \text{g/mol}} $$
- Calculer la fraction molaire de vitamine C
La fraction molaire est calculée comme suit :
$$ \text{Fraction molaire} = \frac{n_{\text{vitamine C}}}{n_{\text{vitamine C}} + n_{\text{maltose}}} $$
Remplaçons par les valeurs précédentes pour obtenir la fraction.
La fraction molaire de vitamine C dans la tablette est approximativement $0.095$.
More Information
La fraction molaire est un concept clé en chimie qui quantifie la proportion d'un composé par rapport à la totalité des composés présents. Cela aide à comprendre les interactions et les proportions des substances dans un mélange.
Tips
- Oublier de convertir toutes les unités en grammes peut mener à des erreurs dans le calcul des moles.
- Ne pas additionner correctement les masses molaires peut également fausser le résultat.
AI-generated content may contain errors. Please verify critical information